تعد السوائل موضوعًا يصعب سبر أغواره. ويجب على علماء الكيمياء الفيزيائية الاهتمام بها نظرًا إلى أن عددًا كبيرًا من التفاعلات الكيميائية يحدث فيها باعتبارها وسطًا للتفاعل لدرجة أن عدم استكشافها ووضع نموذج لخواصها يُعد إغفالاً جسيمًا. وتكمن الصعوبة في فهمها في أنها مرحلة وسيطة بين طرفي نقيض : الاضطراب الفوضوي للجزيئات في الحالة الغازية والمصفوفات الجامدة للذرات في الحالة الصلبة. علاوة على ذلك، يُعد الماء – وهو أهم سائل يجب علينا فهمه – شيئًا غاية في الغرابة لدرجة أن الفهم العميق لخواصه يظل أمرًا مراوغا على نحو كبير.
توجد عدة جوانب للحالة السائلة التي تستهدف دراستها دراسة تجريبية، وتشمل الموضع الذي تتخذه الجزيئات في أي لحظة ومدى سرعة حركتها، ومدى سهولة حركتها بالنسبة إلى بعضها البعض. كما يمكن دراستها أيضًا من خلال رصد انتقال المواد المذابة عبرها ومن خلال رصد الطريقة التي تمتص بها أنواعًا وألوانا مختلفة من الإشعاع الكهرومغناطيسي. ويتطلب كل أسلوب تجريبي، كما هو معهود في الكيمياء الفيزيائية، تصميم نموذج لتفسير النتائج. وعلى عكس الغازات، بالطبع، حيث تكون التفاعلات بين الجزيئات ضئيلة من الوهلة الأولى، تكون التفاعلات في السوائل، حيث تتدافع الجزيئات، محورية للوصف.
حتى مفهوم تحديد موضع وجود الجزيئات ملغز، نظرًا إلى أنها في حركة متواصلة، وتتجاوز بعضها البعض، وتتعرج وتلتف أثناء حركتها. ومن أجل وصف البنية الفعلية لسائل ما، كل ما يمكننا عمله هو تسجيل احتمالية وجود جزيء ما على بعد مسافة معينة من جزيء آخر. ويمكن التوصل إلى معلومات من هذا النوع تجريبيا بالاستعانة بنفس التقنيات المستخدمة مع المواد الصلبة (حيود الأشعة السينية)، وقد وجد أن الجزيء النموذجي محاط بغلاف من الجزيئات الأخرى، ثم تحاط تلك الجزيئات بغلاف أقل تحديدًا؛ وربما حتى يحيط غلاف ثالث أقل تحديدا بتلك الجزيئات (انظر شكل 4–4). والماء، كما في نواح كثيرة أخرى جزيء غريب؛ إذ وجد أن السائل يتكون من مناطق محددة جيدًا نوعًا ما «شبيهة بالثلج» وسط مناطق «شبيهة بالسائل» غير متبلورة ونقطة انطلاق وضع نموذج للسوائل هو التفكير في كيف تتكدس الكرات الصغيرة معًا عند اهتزازها معًا، والسمات العامة للبنى الموضعية للسوائل يمكن تصورها على نحو كبير من خلال الترتيب غير المحكم لكرات معدنية في أوعية.
لدى علماء الكيمياء الفيزيائية عدة طرق لدراسة ديناميكا الجزيئات في السوائل، أي، خواص حركتها والصورة الأقرب لاستحضارها في الذهن هي حشد متدافع من الناس؛ بحيث إذا درست عملية تدفق السائل تحولت الصورة إلى صورة حشد من المتفرجين يتركون استادًا مكتظا. عن آخره بالجماهير.
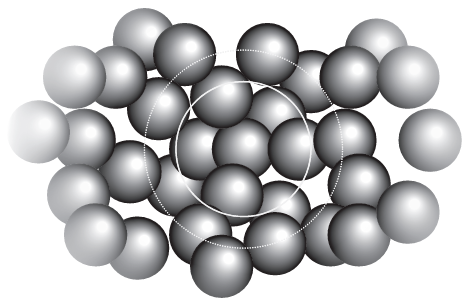
شكل 4–4: صورة توضيحية لبنية سائل ما تتألف من جزيئات كروية الشكل. كل جزيء محاط بغلاف من الجزيئات الأخرى، وهذه الجزيئات يُحيط بها غلاف أقل تحديدا، بل ربما يحيط غلاف ثالث أقل تحديدًا أكثر بتلك الجزيئات والبنية بأكملها متحركة.
تتمثل الطريقة الكلاسيكية لدراسة حركة الجزيئات في قياس درجة «لزوجتها»، أي، مقاومتها للتدفق عبر نطاق من درجات الحرارة. ومع ذلك، من الصعب تفسير اللزوجة على الرغم من أهميتها العملية الكبيرة، كما هي الحال عند تصميم. منشأة كيميائية حيث تُجبر السوائل على التدفق عبر أنابيب من مكان إلى آخر. وتُدرس حركة الجزيئات نفسها من خلال مجموعة متنوعة من التقنيات إحدى هذه التقنيات هي «التشتت النيوتروني»: توجه تيارات من أقارب البروتونات عديمة الشحنة، أي النيوترونات، نحو عينة السائل، وترتد عن جزيئات السائل بمستويات طاقة مختلفة. ومن خلال فحص تلك المستويات، يمكن تكوين صورة عن حركة الجزيئات وتحديد مجموعات الجزيئات المتعاونة التي تعمل بطريقة متناسقة. ويمكن أيضًا لذلك الجسيم النافع الآخر، الفوتون، الذي يُطلق من أجهزة الليزر، أن يوفر معلومات من نوعية مماثلة.
أود هنا أن أشير إلى «الرنين المغناطيسي النووي» إشارة عابرة، بما أنه تقنية أخرى يمكن الاستعانة بها لدراسة حركة الجزيئات في السوائل. ويمكن الاستعانة به على وجه الخصوص لدراسة كيف تدور الجزيئات في الوسط الكثيف والمقيد داخل سائل ما. ووجد أنه في بعض الحالات تدور الجزيئات في سلسلة من الخطوات الصغيرة، متخذة خطوات كثيرة لتدور بالكامل، في حين أنه في بعض السوائل قد يتأرجح الجزيء بزاوية قائمة أو نحو ذلك في كل خطوة.
لقد اهتم علماء الكيمياء الفيزيائية بشدة ببناء النماذج الخاصة بالمواد المذابة في الماء واستخدام تلك المواد الدراسة ديناميكية الحركة الجزيئية. وللمذابات الأيونية (تأمل كلوريد الصوديوم في الماء، مع انتشار أيونات Na+ وCI– بين جزيئات الماء) فائدة خاصة في هذا الصدد نظرًا إلى أنه يمكن سحب الأيونات عبر المذيب من خلال إنشاء مجالات كهربائية وفحص المعدل الذي تتحرك به من خلال رصد التيار الكهربائي الناتج. ويُحصل على بعض النتائج غير المعقولة في البداية. ومن ثم، يلاحظ أن الأيونات الكبيرة تنتقل بسهولة أكبر من الأيونات الصغيرة. وأدت تلك الملاحظة إلى صورة كانت الأيونات تُعتبر فيها محاطة بجزيئات الماء التي تلتصق بها وتجعلها تبدو أكبر نظرًا إلى أن المجموعة بأكملها يجب أن تنتقل عبر السائل. وتجتذب الأيونات الصغيرة جزيئات الماء على نحو أقوى من الأيونات الكبيرة (مما يسفر عنه تكوين مجال كهربائي أقوى)، وبالتالي عندما تحيط بها جزيئات الماء فإنها تبدو كأنها أيونات أكبر حجمًا.
فند هذا النموذج الخاصة بحركة الأيونات عبر الماء على نحو شبه تام حين وجد أن أيونات الهيدروجين – الأيونات الأصغر على الإطلاق – كانت الأسرع على الإطلاق، ومن ثُم هي بعيدة تماما عن التصرف مثلما تتصرف الأيونات الصغيرة والتحرك ببطء عندما تحيط بها جزيئات ماء كثيرة! أعطى التفسير نظرة ثاقبة على سلوك البروتونات في الماء؛ إذ جرى استنتاج أنها لم تكن تتحرك فعليًّا على الإطلاق. وبدلًا من ذلك، ثمة انتقال فعلي لبروتون مع حدوث تغير في ملكية جزيئات الماء المجاورة للبروتونات الخاصة بها. لذا، في سلسلة من جزيئات الماء كهذه:

ويظهر البروتون فجأة وبفعالية على الطرف الآخر من السلسلة ولا يوجد انتقال فعلي متثاقل للبروتون الأصلي.
ما زال علماء الكيمياء الفيزيائية يستعينون بنموذج مبكر لبنية محاليل الأيونات في الماء حتى اليوم باعتباره أول مقاربة لسلوك الأيونات في المحلول ولا سيما خواصها الديناميكية الحرارية. اقترح هذا النموذج كل من بيتر ديباي (1884–1966) وإريش هوكل (1896–1980)، في عام 1923، وهو في رأيي، يُعد نموذجًا ممتازا لعملية بناء النماذج؛ إذ إنه يشمل الكثير من الخطوات الصغيرة التي كل منها تسترشد بفكرة ثاقبة من علم الفيزياء تتمثل الفكرة الأساسية في أن الكاتيون (الأيون الموجب الشحنة) في المحلول يكون مُحاطًا عادةً بالأنيونات (الأيونات السالبة الشحنة)، والعكس صحيح. وهكذا، إذا فكرنا في الأمر من حيث متوسط الوقت الخاص ببيئاتها، فإن كل أيون محاط بـ «وسط أيوني» دقيق له شحنة معاكسة والتفاعل الخاص بالأيون الأساسي مع الوسط الذي له شحنته المعاكسة يقلل من طاقته وبالتالي يجعله أقل نشاطًا من الناحية الديناميكية الحرارية.
طور ديباي وهوكل هذا النموذج كميًّا واستنتجا ما صار يُعرف بـ «قانون ديباي–هوكل» والذي فيه يتناسب انخفاض الطاقة مع الجذر التربيعي لتركيز الأيونات الموجودة. في الواقع، هذا مثال آخر للقوانين المقيدة التي تميز الكيمياء الفيزيائية: في هذه الحالة، تعني القيم التقريبية المستخلصة في خضم تطويره أنها صحيحة تمامًا في حالة التركيز الصفري. وعلى الرغم من ذلك القصور، يُعد هذا القانون نقطة انطلاق جيدة لنظريات أكثر تطورًا عن المحاليل الأيونية.
