


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
أقرأ أيضاً
التاريخ: 4-7-2016
التاريخ: 18-2-2016
التاريخ: 2023-10-19
التاريخ: 24-4-2016
|
رأينا في الفصل الثالث سلسلة من التفاعلات غير المتجانسة تؤدي إلى نقص واسع النطاق في أوزون الستراتوسفير في أثناء الربيع القطبي. وعلى غرار ذلك يمكن إنتاج حمض الكبريت بسيرورة غير متجانسة حينما تكون المتفاعلات اللازمة متوفّرة في قطيرات الغيم.
بالابتداء مرة أخرى بثاني أكسيد الكبريت، تحصل التفاعلات التالية:
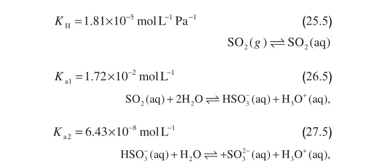
وعلى غرار ثاني أكسيد الكربون، تعتمد قابلية انحلال ثاني أكسيد الكبريت في الماء على عامل الحموضة pH ، لكنها أكبر كثيراً على كامل مجال عامل الحموضة. فإذا كانت نسبة المزج الجوية لثاني أكسيد الكبريت تساوي ppby 10 عند ضغط يساوي °P ، كانت قابلية انحلاله في الماء 6-10×molL-1 2.2 عندما يساوي عامل حموضة المعلقات الجوية 4.0، و-1 2.2x10-3 molL عندما يساوي 7.0. إن قابلية الانحلال في الماء هي واحد من العوامل التي تؤثّر في معدل التفاعل غير المتجانس. وتحصل أكسدة أجناس الكبريت ضمن قُطيرات الماء. وأهم المؤكسدات هو فوق أكسيد الهدروجين، وهو مادة كيميائية نسبة مزجها الجوية تساوي 1 أو 2ppbv وتنحل في الماء بسهولة
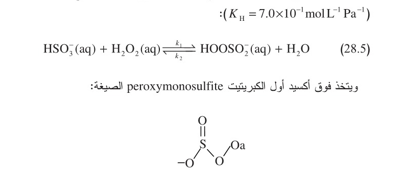
التي يتغيَّر ترتيبها بسهولة لتكوين كبريتات الهدروجين HSO ذي البنية التالية:


ينطبق قانون المعدل هذا على الحالات التي تكون فيها قيمة عامل الحموضة بين 2 و 5 تقريباً ويكون كبريتيت الهدروجين -HSO3 هو جنس الكبريت IV المائي الرئيسي.
ضمن هذا المجال، تكون أكسدة ثاني أكسيد الكبريت بفوق أكسيد الهدروجين هي الآلية المهيمنة ويكون معدل التفاعل مستقلاً عن عامل الحموضة تقريباً. وتحت القيم 2 - pH ، يتناقص المعدل بسبب تزايد قيمة مقام المعادلة 34.5 وعند قيم 2 ~pH أعلى، يُصبح الكبريتيت SO جنس الكبريت المهيمن، ويتناقص معدل الأكسدة بواسطة هذا المؤكسد لأنه لا يتفاعل مع فوق أكسيد الهدروجين.
ويتضمن مسار آخر غير متجانس الأوزون مؤكسداً . في هذا الحالة يكون كل من كبريتيت الهدروجين وأيونات الكبريتيت قابلين للأكسدة:
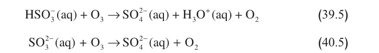
في التفاعلات القائمة على الأوزون، وبأخذ السيرورات السابقة في الحسبان، يكون فوق أكسيد الهدروجين هو المؤكسد الرئيسي عندما 5.5>PH، ويكون الأوزون أكثر أهمية عند قيم عامل الحموضة الأخرى. وتبعاً لتوفر المواد المؤكسدة، يمكن للتفاعلات غير المتجانسة ان تساهم في اكسدة الكبريت بمقدار اكبر مما يساهم به سيروات الطور الغازي
Considerations, Acid Precipitation Series; v. 3 (Boston, MA: Butterworth = Publishers, 1984).


|
|
|
|
حقن الذهب في العين.. تقنية جديدة للحفاظ على البصر ؟!
|
|
|
|
|
|
|
علي بابا تطلق نماذج "Qwen" الجديدة في أحدث اختراق صيني لمجال الذكاء الاصطناعي مفتوح المصدر
|
|
|
|
|
|
|
ضمن برنامج تأهيل المنتسبين الجدد قسم الشؤون الدينية يقدم محاضرات فقهية وعقائدية لنحو 130 منتسبًا
|
|
|