
تركيب هاليدات الأريل و الفاينيل
 المؤلف:
أ. د محمد مجدي واصل
المؤلف:
أ. د محمد مجدي واصل
 المصدر:
اساسيات الكيمياء العضوية
المصدر:
اساسيات الكيمياء العضوية
 الجزء والصفحة:
ص 279-280-281-282
الجزء والصفحة:
ص 279-280-281-282
 2023-08-19
2023-08-19
 2280
2280
من الملاحظ أن تراكيب هاليدات الأريل والفاينيل يشتركان في أن ذرة الهالوجين في كلا المركبين تتصل بمركز غير مشبع ( SP2 ) وفي هذا يختلفان عن هاليدات الألكيل التي تتصل فيها ذرة الهالوجين إلى مركز مشبع (SP3) .
فمثلاً في كلورو بنزين وكلوريد فايئيل يتضح أن ذرة الكلور متصلة إلى ذرة كربون ثلاثية (SP2) بينما كلوريد البنزيل وكلوريد الأليل فإن ذرات الكلور تتصل بذرات كاربون هرمية رباعية (SP2) . كما يلي :

ويرجع سبب قلة فعالية هاليدات الأريل والفاينيل تجاه تفاعلات الإزاحة النيوكليوفيلية إلى عاملين مختلفين أولهما عدم تمركز الالكترونات أي انتشارها من خلال ظاهرة الرئين والثاني الاختلاف في طاقات الرابطة σ بسبب اختلاف تهجين ذرة الكاربون .
ولنعد إلى التراكيب ثانية فإننا يمكننا ملاحظة أن الكلورو بنزين هو ليس هجيناً لتركيبي كيكولي المعروفين ( 1 و 2 ) فقط بل أنه هجين أيضاً لثلاثة تراكيب ( 3 ، 4 ، 5 ) فيهما تكون ذرة الكلور حاملة لشحنة موجبة ومرتبطة إلى ذرة الكاربون برابطة مزدوجة وإنه توجد شحنات سالبة في مواقع اورثو وبارا - بالنسبة للهالوجين وكما يلي :

كذلك فإن لكلوريد فاينيل تركيبين هجينين أولهما الاعتيادي ( 6 ) والآخر فيه تكون ذرة الكلور حاملة لشحنة موجبة ومرتبطة بذرة الكاربون برابطة مزدوجة وأن ذرة الكاربون رقم 2 حاملة لشحنة سالبة ( 7 ) هذا التركيب يشبه في خواصه التراكيب الهجينية للكلورو بنزين ( 3 ، 4 ، 5 ) .

وهذه التراكيب الهجينية مثل 3 ، 4 ، 5 ، 7 توضح أن ذرة الكلور مرتبطة بذرة الكاربون برابطة تتشأ من مساهمة لأكثر من زوج من الالكترونات ، يعني أنها أقوى من أن تكون رابطة منفردة نقية .
ويعني أن هذه التراكيب مستقرة بالرنين وأن هذا النوع من الاستقرارية سيزيد طاقة التنشيط لتفاعل الإزاحة وبالتالي يبطئ التفاعل ، وعليه فأن تفاعل مثل هذه المركبات بتفاعلات تتضمن إزاحة ذرة هالوجين سيكون أبطأً من تفاعلات هاليدات الألكيل مثل كلوريد البنزيل مثلاً والذي لا يمكن فيه كتابة تراكيب هجينية عدا تلك الخاصة بتراكيب كيكولي (8،9) .
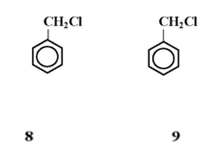
والتعليل الآخر لقلة الفعالية يمكن أن يرجع إلى الاختلاف في نوع ذرات الكاربون المتصل بها الهالوجين . قفي هاليدات الألكيل مثل كلوريد البنزيل وكلوريد الأليل فأن ذرة الكاربون الحاملة للهالوجين تنشأً من مدارات SP3 المهجنة .
بينما في كلورو بنزين وكلوريد الفاينيل فهي ناشئة عن مدارات SP2 المهجنة وبالتالي فهي أقصر وأقوى وعليه فإنها تحتاج إلى ظروف أكثر قوة لكي تتفاعل بالمقارنة مع هاليدات الألكيل .
من الأدلة التي تؤيد صحة التوقعات المسببة لقلة الفعالية هي طول الرابطة فلقد وجد بأن طول رابطة C-Cl في كلوريد الفاينيل وكلورو بنزين هي 1.69 أ مقارنة بطول رابطة C-Cl في العديد من كلوريدات الألكيل والتي تتراوح بين 1.77 - 1.80 أ بالمثل فإن رابطة C-Br في برومو بنزين وبروميد فاينيل هي 1.86 أ مقارنة بطول رابطة C-Br في العديد من بروميدات الألكيل والتي تتراوح بين 1.91 - 1.92 أ .
 الاكثر قراءة في مواضيع عامة في الكيمياء العضوية
الاكثر قراءة في مواضيع عامة في الكيمياء العضوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة


