

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
التشكيل الالكتروني. مبدأ الاستبعاد لباولي
المؤلف:
Robert T. Morrison & Robert. N Boy
المصدر:
الكيمياء العضوية Organic chemistry
الجزء والصفحة:
p 8 6th ed
31-10-2016
5340
التشكيل الالكتروني. مبدأ الاستبعاد لباولي
Electronic configuration. Pauli exclusion principle
هنالك عدد من القواعد التي تعين كيفية توزع الالكترونات في الذرة، أي تعين التشكيل الالكتروني لذرة ما. إن أهم هذه القواعد هو مبدأ الاستبعاد الذي وضعه العالم باولي، وبنص: أنه لا يمكن لأكثر من الكترونين شغل أي مدار ذري واحد، ويجب أن يكون لهذين الالكترونين لفان (برمان) ذاتيان متعاكسان (spins). ويقال عن الالكترونين اللذين لهما لف ذاتي متعاكس أنهما متزاوجان، أما الالكترونان المتماثلان باللف الذاتي فيميلان الى الابتعاد بعضهما عن بعض قدر المستطاع. وهذا الميل هو الأكثر الأهمية من بين العوامل التي تعين أشكال وخواص الجزيئات.
لقد طور مبدأ الاستبعاد العالم ولفغانغ باولي الابن في عام 1925 (في معهد الفيزياء النظرية، هامبورغ، ألمانيا) وقد دعي حجر الزاوية في الكيمياء.
يعطينا الجدول 1.1 التشكيل الالكتروني للعناصر العشرة الأولى في الجدول الدوري ويمكن أن نرى أن المدار الالكتروني لا يشغل قبل أن تمتلئ المدارات ذات الطاقة الأدنى منه (مثلا يمتلئ 2s بعد 1s، و 1s، و 2p بعد 2s).
الجدول 1.1: التشكيل الالكتروني
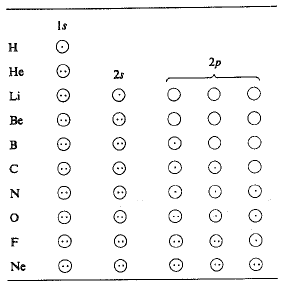
ونلاحظ، كذلك، أن مداراً ما لا يشغل بزوجين من الالكترونات حتى تشغل المدارات الأخرى ذات الطاقة المتكافئة له بالكترون واحد (المدارات 2p مثلا). تؤلف الالكترونات 1s الطبقة shell الأولى التي تستوعب الكترونين، تتألف الطبقة الثانية التي تتسع لثمانية الكترونات من المدارات 2s و 2p. العناصر التي تلي العشرة الأولى فإنها تحوي طبقة ثالثة تتألف من المدارات 3s والمدارات 3p، وهكذا.
 الاكثر قراءة في مواضيع عامة في الكيمياء العضوية
الاكثر قراءة في مواضيع عامة في الكيمياء العضوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















