


 الفيزياء الكلاسيكية
الفيزياء الكلاسيكية
 الكهربائية والمغناطيسية
الكهربائية والمغناطيسية
 علم البصريات
علم البصريات
 الفيزياء الحديثة
الفيزياء الحديثة
 النظرية النسبية
النظرية النسبية
 الفيزياء النووية
الفيزياء النووية
 فيزياء الحالة الصلبة
فيزياء الحالة الصلبة
 الليزر
الليزر
 علم الفلك
علم الفلك
 المجموعة الشمسية
المجموعة الشمسية
 الطاقة البديلة
الطاقة البديلة
 الفيزياء والعلوم الأخرى
الفيزياء والعلوم الأخرى
 مواضيع عامة في الفيزياء
مواضيع عامة في الفيزياء|
أقرأ أيضاً
التاريخ: 31-8-2017
التاريخ: 15-2-2016
التاريخ: 2024-01-25
التاريخ: 29-11-2020
|
تكافئ التكلفة والطاقة
في أوائل هذا القرن توصل ألبرت أينشتين إلى المعادلة E = mc2 أثناء بلورة نظرية النسبية. ومن بين كل معادلات الفيزياء ربما كانت هذه المعادلة اكثرها بساطة ومن ثم أكثرها شهرة بين عامة الناس. ولكن ماذا تعني هذه العبارة البسيطة والعميقة في آن واحد ؟
أولاً: أن c ترمز لسرعة الضوء وتساوي 3×108 ،و هذا عدد كبير جداً ويزداد كبراً عند تربيعه. أما الرمز m فيمثل كتلة جسم او مجموعة من الأجسام ، بينما يرمز الحرف E إلى كمية الطاقة. تقول العبارة E = mc2 أن هناك طاقة تسمى الطاقة الكتلية مرتبطة بوجود المادة. فمثلاً ، كمية الطاقة التي تمتلكها كتلة قدرها 1 kg هي:

ومع ذلك فإن إجراء هذه العملية الحسابية لا يعطي أي فكرة متعمقة عن صورة هذه الاقة أو كيفية تفسير هذه المعادلة.
قد يكون من المفيد في هذا الشأن النظر بإمعان إلى تركيب المادة. تتكون المواد التي نتعامل معها في حياتنا اليومية من ذرات مختلف العناصر الكيمائية المترابطة مع بعضها البعض في صورة جزيئات بقوى كهرومغناطيسية ، ويمكن أن تتغير البنية الجزيئية للمادة نتيجة للتفاعلات الكيميائية كالاحتراق مثلاً. وعند ترتيب الذرات على هيئة جزيئات تبذل قوى الترابط شغلاً وهذا يؤدي إلى تغير طاقة جهد النظام. تذكر أن طاقة الجهد تنشأ نتيجة لمواضع او هيئة الأجسام المتفاعلة. وعليه فإن التغير في البنية الجزيئية هو تغير في الهيئة ، ويمثل بالتالي تغيراً في طاقة جهد الجزء، وهو ما يسمى طاقة الارتباط.
عندما تكون الذرات في البنية الجزيئية الجديدة أشد ترابطاً مما كانت قبل إعادة توزيعها تقل طاقة جهد النظام ، وتنبعث الطالقة من النظام في صورة حرارة أو ضوء عادة. اما إذا كان التفاعل ينتج جزيئات جديدة ذات ذرات أقل ترابطاً فإن النظام لابد أن يكتسب بعض الطاقة ، ربما في صورة حرارة.
تعنى معادلة اينشتين التي تربط الكتلة بالطاقة ان التغيرات في طاقة النظام يصحبها تغيرات في كتلة النظام ، ويمكن كتابة المعادلة E = mc2 في الصورة البديلة الآتية:
(1) 
من المعلوم ان القيمة النمطية للطاقة المتحررة نتيجة للاحتراق الكامل لأنواع الوقود العادي حوال 107 Jلكل kg من المادة الداخلة في التفاعل ( الوقود زائد الاوكسجين). بماذا تخبرنا معادلة أينشتين عن مقدار التغير في كتلة كل كيول جرام من المادة عند احتراقه؟ تخبرنا المعادلة (1) أن كل كيلو جرام من الكتلة يتغير بمقدار:
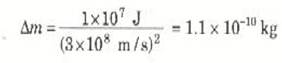
وعليه فإن التفاعل الكيميائي النمطي يمكن أن يغير كتلة المواد المتفاعلة بما يعادل جزءاً واحداً من شعرة بلايين جزء ، وهذا التغير في الكتلة لا يمكن قياسه بأكثر الطرف ضباطية في الوقت الحالة. وهكذا فإننا في خبراتنا اليومية مع التفاعلان الكيميائية لا نحس إطلاقاً بأي تغير في الكتلة.
ولكن عند دراسة الأنوية الذرية سنجد أن البروتونات والنيوترونات ، والتي تسمى بالجسيمات الأولية ، مترابطة مع بعضها البعض بقوة ترابط نووي أشد كثيراً من القوى الكهرومغناطيسية بين الذرات. كذلك فإن التفاعلات الكيميائية لا تغير هذه البني النووية ، ولكن التفاعلان النووية كالانشطار والاندماج تغيرها. والانشطار هو عملية تنشق فيها الأنوية الثقيلة كاليورانيوم والبلوتونيوم إلى شظايا أخف ، وهي مصدر الطاقة في المفاعلات النووية الحالية. أما الاندماج فيتضمن التصاق واندماج الأنوية الخفيفة مكونة بني نووية أكثر تعقيداً. ومن أهم التفاعلات الاندماجية النووية اندماج أربع أنوية أيدروجين لتكوين نواة هيليوم واحدة ، وهذا هو المصدر الرئيسي لتوليد الطاقة في الشمس.
عند قياس الكتلة الكلية قبل وبعد التفاعل النووي الانشطاري أو الاندماجي بعناية شديدة سوف نجد أنها قد نقصت نقصاً كبيراً. علاوة على ذلك فغن هذا النفص في الكتلة يرتبط بالطاقة المتحررة في التفاعل بصورة تتفق تماماً مع المعادلة (1). ففي حالة الانشطار سنجد ان حوالي 0.1 في المائة من الكتلة الأصلية للنواة الثقيلة يتحول إلى طاقة ، بينما ترتفع هذه النسبة إلى 0.8 في المائة تقريباً في حالة الاندماج ومن الواضح أن هاتين القيمتين تمثلان تغيراً محسوساً في الكتلة ، بعكس ما يحدث في التفاعلات الكيميائية النمطية. وهكذا فإن كمية الطاقة المتحررة في التفاعلات النووية لكل كيلو جرام من المادة المتفاعلة أكبر من نظيرتها في التفاعلات الكيميائية بمقدار 10 إلى 100 مليون مرة تقريباً.
يمكن حدوث التحول النهائي للمادة إلى طاقة إذا وجدت عملية ما تختفي فيها الكمية الابتدائية من المادة تماماً وتحل محلها طاقة إشعاعية صرفة ( ضوء) عديمة الكتلة هذا التحول بنسبة 100 في المائة شوهد بالفعل في المختبر في عملية تسمى فناء المادة وضديد المادة. ذلك أن لكل جسيم اولي نسخة ضديدة مطابقة لا توجد في حالة مستقرة، ولكنها تتكون لفترات وجيزة في التفاعلات النووية. وعلى سبيل المثال يمكننا ذكر ضديد الإلكترون ، أو البوزيترون ، وهو جسيم له نفس الخصائص الفيزيائية المميزة للإلكترون باستثناء شحنته الكهربائية فهي موجبة. وعندما يتصادم الإلكترون والبوزيترون ينتهي وجودهما تماماً ويخلق بدلاً منهما شعاعان من أشعة جاما عديمة الكتلة. وهي طاقة إشعاعية ( او ضوء) ذات طول موجبة قصيرة جداً. وبمقياس الطاقة الكلية لشعاعي جاما وجد أنها تساوي بالضبط الكتلة الكلية الأصلية للإلكترون والبوزيترون مضروبة في c2.
كذلك أمكن مشاهدة العملية العكسية ، أي خلق أزواج المادة وضديد المادة من إشعاع جاما صرف. هذه النتائج تمثل تحقيقاً أكيداً لا شك فيه لنظرية أينشتاين النسبية.



|
|
|
|
حقن الذهب في العين.. تقنية جديدة للحفاظ على البصر ؟!
|
|
|
|
|
|
|
علي بابا تطلق نماذج "Qwen" الجديدة في أحدث اختراق صيني لمجال الذكاء الاصطناعي مفتوح المصدر
|
|
|
|
|
|
|
ضمن برنامج تأهيل المنتسبين الجدد قسم الشؤون الدينية يقدم محاضرات فقهية وعقائدية لنحو 130 منتسبًا
|
|
|