

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
معايرات المعقدات
المؤلف:
د.عبدالله محمود ابو الكباش
المصدر:
الكيمياء التحليلية المفاهيم الاساسية في التحليل التقليدي والالي
الجزء والصفحة:
ص 109
2024-02-05
1322
إن معظم أيونات المعادن بإمكانها استقبال زوج من الإلكترونات من أيون آخر، أو من جزيء به ذرة عليها إلكترونات حرة فتنشأ رابطة تساهمية من طرف واحد (Coordinate covalent bond). والأيون أو الجزيء الذي يحتوي على ذرة تعطي زوج الإلكترونات تسمى المعطي (Ligand) ، والمركب الناتج يسمى المعقد (Complex)، ويمكن تشبيه الإلكترونات المنبثقة من المعطي بالسن، ويكون المعطي أحادي السن إذا ساهم بزوج واحد من الإلكترونات (mono dentate) ، وإذا ساهم بزوجين فيسمى (bidentate)، وهكذا إذا كانت أزواج الإلكترونات المشتركة كثيرة
فيسمى (Polydentate ligand).
وكمثال على تكون المعقدات يُعَدُّ الماء معطياً ممتازاً، ويتفاعل ليكون أيوناً مائياً، فمثلاً أيون النحاس يتفاعل مع أربعة جزيئات من الماء كما يلي:

ويسمى عدد الجزيئات المعطية التي تتحد مع أيون المعدن بالعدد التساهمي. وعلى هذا فأيون النحاس عدده التساهمي 4 إذ إنه يتحد مع أربعة جزيئات ماء، وجزيء الماء هذا يُعَدُّ معطياً أحادي السن مثله مثل جزيء الأمونيا. NH3 وهناك أيونات أيضاً تُعَدُّ أحادية السن مثل - CN-، F- ، Cl- ، OH ، والمعطيات ثنائية السن
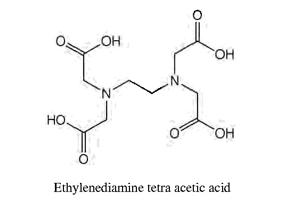
مثل -NH2 CH2 CH2NH2 ويسمى إيثيلين ثنائي الأمين (Ethylene diamine) ومن أشهر هذه (ethylenediamine tetra acetic acid) (EDTA) .
 الاكثر قراءة في مواضيع عامة في الكيمياء التحليلية
الاكثر قراءة في مواضيع عامة في الكيمياء التحليلية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















