
Possible charges: Naming ions with multiple oxidation states
 المؤلف:
John T. Moore, EdD
المؤلف:
John T. Moore, EdD
 المصدر:
Chemistry Essentials For Dummies
المصدر:
Chemistry Essentials For Dummies
 الجزء والصفحة:
p 60
الجزء والصفحة:
p 60
 1-1-2017
1-1-2017
 2911
2911
Possible charges: Naming ions with multiple oxidation states
The electrical charge that an atom achieves is sometimes called its oxidation state. Many of the transition metal ions (the B families) have varying oxidation states because these elements can vary in how many electrons they lose. Table 1-1 shows some common transition metals that have more than one oxidation state. elements can vary in how many electrons they lose. Table 1-1 shows some common transition metals that have more than one oxidation state.
Table 1-1: Common Metals with More than One Oxidation State
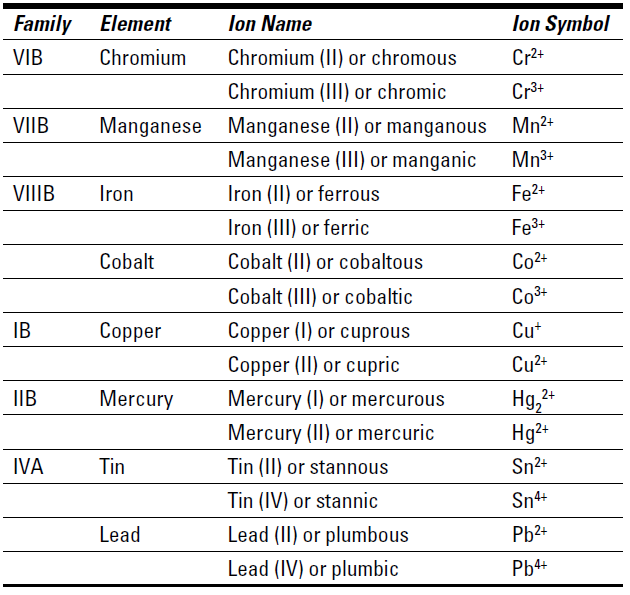
Notice that these cations can have more than one name. Here are two ways to name cations of elements that have more than one oxidation state:
✓ Current method: Use the metal name, such as chromium,
followed by the ionic charge written as a roman numeral in parentheses, such as (II). For example, Cr2+ is chromium (II) and Cr3+ is chromium (III).
✓ Traditional method: An older way of naming ions uses -ous and -ic endings. When an element has more than one ion, do the following:
• Give the ion with the lower oxidation state (lower numerical charge, ignoring the + or –) an -ous ending.
• Give the ion with the higher oxidation state (higher numerical charge) an -ic ending. So for chromium, the Cr2+ ion is named chromous and the Cr3+ ion is named chromic.
 الاكثر قراءة في مواضيع عامة في الكيمياء اللاعضوية
الاكثر قراءة في مواضيع عامة في الكيمياء اللاعضوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة


