

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
The Main-Group Elements: Bonding and Properties
المؤلف:
LibreTexts Project
المصدر:
................
الجزء والصفحة:
.................
5-6-2020
2075
The Main-Group Elements: Bonding and Properties
As we begin our summary of periodic trends, recall that the single most important unifying principle in understanding the chemistry of the elements is the systematic increase in atomic number, accompanied by the orderly filling of atomic orbitals by electrons, which leads to periodicity in such properties as atomic and ionic size, ionization energy, electronegativity, and electron affinity. The same factors also lead to periodicity in valence electron configurations, which for each group results in similarities in oxidation states and the formation of compounds with common stoichiometries.
The most important periodic trends in atomic properties are summarized in Figure .1 . Recall that these trends are based on periodic variations in a single fundamental property, the effective nuclear charge (Zeff), which increases from left to right and from top to bottom in the periodic table.
The diagonal line in Figure .1 separates the metals (to the left of the line) from the nonmetals (to the right of the line). Because metals have relatively low electronegativities, they tend to lose electrons in chemical reactions to elements that have relatively high electronegativities, forming compounds in which they have positive oxidation states. Conversely, nonmetals have high electronegativities, and they therefore tend to gain electrons in chemical reactions to form compounds in which they have negative oxidation states. The semimetals lie along the diagonal line dividing metals and nonmetals. It is not surprising that they tend to exhibit properties and reactivities intermediate between those of metals and nonmetals. Because the elements of groups 13, 14, and 15 span the diagonal line separating metals and nonmetals, their chemistry is more complex than predicted based solely on their valence electron configurations.
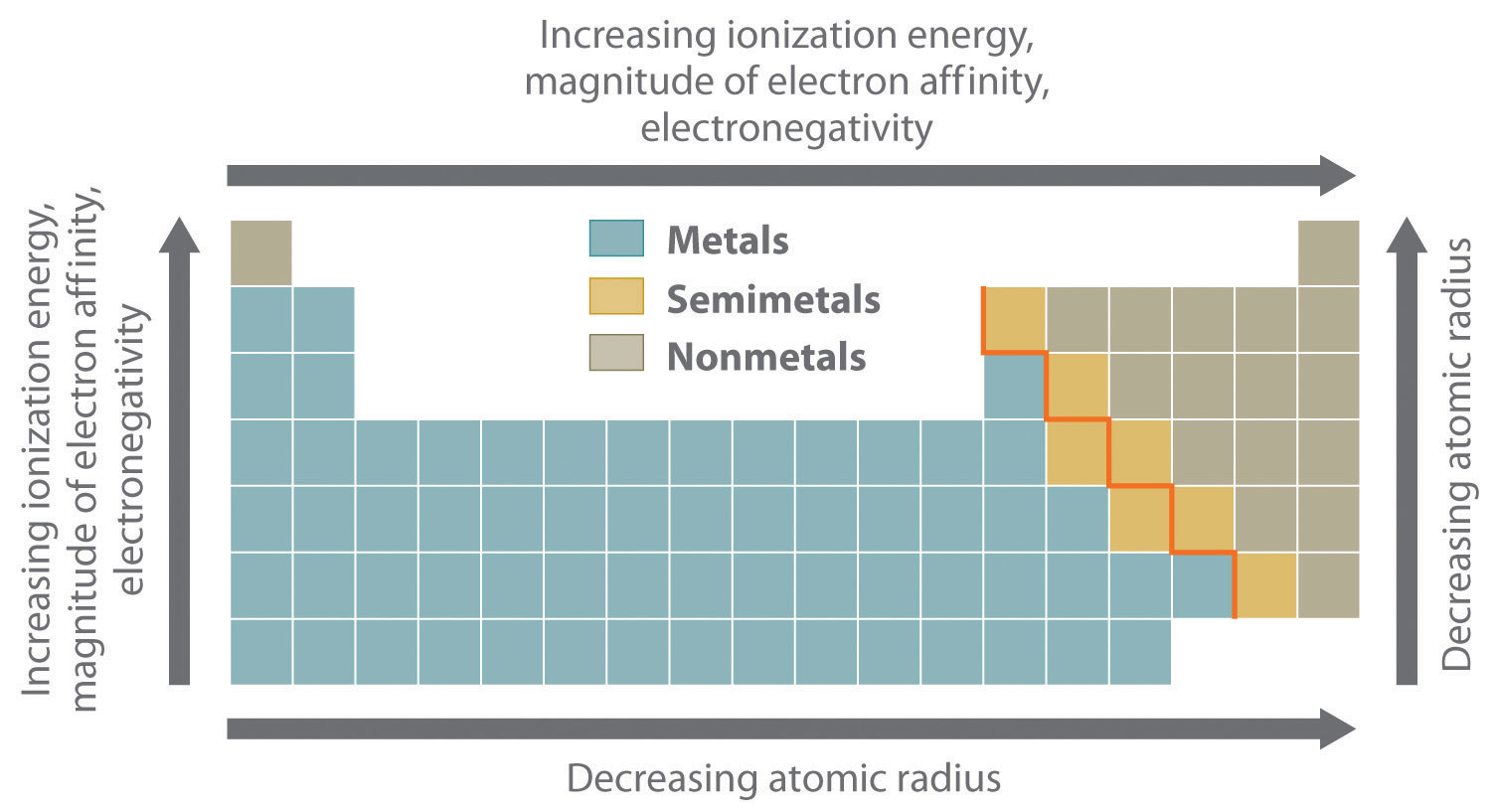
Figure .1 : Summary of Periodic Trends in Atomic Properties. Ionization energies, the magnitude of electron affinities, and electronegativities generally increase from left to right and from bottom to top. In contrast, atomic size decreases from left to right and from bottom to top. Consequently, the elements in the upper right of the periodic table are the smallest and most electronegative; the elements in the bottom left are the largest and least electronegative. The semimetals lie along the diagonal line separating the metals from the nonmetals and exhibit intermediate properties.
 الاكثر قراءة في مواضيع عامة في الكيمياء اللاعضوية
الاكثر قراءة في مواضيع عامة في الكيمياء اللاعضوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















