
الانتروبيا Entropy
 المؤلف:
محمد عطية سويلم، د. محمد روبين إدريس، بديع صالح الخطيب، د. أحمد يوسف قواسمة
المؤلف:
محمد عطية سويلم، د. محمد روبين إدريس، بديع صالح الخطيب، د. أحمد يوسف قواسمة
 المصدر:
الفيزياء العامة
المصدر:
الفيزياء العامة
 الجزء والصفحة:
ص 279
الجزء والصفحة:
ص 279
 9-12-2019
9-12-2019
 2298
2298
الانتروبيا Entropy
يعتبر القانون الأول للديناميكا الحرارية قانون الطاقة. أما القانون الثاني للديناميكا الحرارية ، فهو قانون الإنتزوبيا ، وكل عملية تحدث في الطبيعة سواء كانت ميكانيكية أو كهربائية أو كيميائية ، أو بيولوجية يجب أن يتفق حدوثها ، وينسجم مع هذين القانونين .
أنه عند انتقال الجسم من حالة لأخرى، فإن الفرق بين كمية الحرارة المضافة والشغل المبذول (Q-W) . ثابت ، ولا يعتمد على المسار من الحالة الأولى إلى الثانية . ولقد اعتبر هذا الفرق بانه يساوي التغير في الطاقة الداخلية للجسم في أثناء انتقاله من المحالة الأولى إلى الحالة الثانية .
ويمكن تعريف الإنتزوبيا بنفس الطريقة ، فلو أخذنا حالتين لنظام ما ، ويربط بين هاتين الحالتين عدة مسارات لعمليات منعكسة ، فإننا نجد انه عند قسمة كمية الحرارة عند كل نقطة على المسار على درجة الحرارة المطلقة للنظام عند تلك النقطة ، وجمعنا ناتج القسمة عند جميع نقاط المسار ، فإن هذا المجموع لا يتغير بتغير المسار، علما أن كمية الحرارة المضافة عبر المسار تختلف من مسار لآخر ، ونعبر عن نلك بالعلاقة الرياضية التالية :
………………(1) 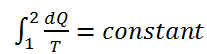
ويسمى هذا المفهوم (الإنتروبيا) ، ويرمز له بالرمز (S) . وعليه فإن :
(2)........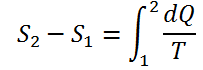
وإذا كان التغير في الإنتروبيا بين الحالتين صغيراً جداً ، فإن العلاقة تصبح :
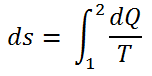
ووحده الإنتروبيا هي سعر / درجة مطلقة (Cal/°k) أو جول/ درجة مطلقة (Joule/°k) .
 الاكثر قراءة في الديناميكا الحرارية
الاكثر قراءة في الديناميكا الحرارية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة


