


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
أقرأ أيضاً
التاريخ: 6-2-2016
التاريخ: 2023-11-02
التاريخ: 2023-11-07
التاريخ: 2023-10-09
|
مع أن غاز ثاني أوكسيد الكبريت لا يمتلك تأثيراً ساماً جداً، إلا أنه عند مستويات منخفضة يكون له تأثير على الصحة بشكل عام، وأحد العناصر الأساسية المسببة للتلوث الجوي . حيث يعد بعضهم أن تعيين تركيز هذا الغاز (أي تحليله كميائياً) في الهواء معياراً كافياً بذاته لتقدير مدى التلوث الجوي. إن تأثير غاز ثاني أوكسيد الكبريت الأساسي هو على الجهاز التنفسي، مسبباً التخرش وإضعاف مقاومة المجاري التنفسية، خاصة للأشخاص ضعيفي البنية والمصابون بالربو التحسسي حيث يؤدي إلى صعوبة التنفس، ومن الدلائل على تلوث الجو بغاز ثاني أوكسيد الكبريت هو تحريض إفراز اللعاب. إن التراكيز المسموح بها من SO2 والتي تعد مقبولة هي من رتبة 0.6 ميلي غرام / متر مكعب من الهواء.
إن تركيزاً محدداً لغاز SO2 في جو هواؤه نقي، يكون ذا تأثير أقل أذى بكثير فيما لو وجد هذا الغاز بالتركيز نفسه مع أدخنة و ملوثات أخرى. ذلك أن غاز ثاني أوكسيد الكبريت الذي يتثبت على جسيمات الغبار والكربون يُحفِّز في الواقع ليتحول مشكلاً حمض الكبريت الذي قد يؤثر على الحويصلات الرئوية، في حين أن ثاني أوكسيد الكبريت الغازي، وبسبب انحلاله باللعاب الفموي، يتم طرحه، بصورة طبيعية، عند 95% من الأشخاص أصحاء البنية.
عند تراكيز مرتفعة من غاز SO2 (أعلى منppm 500)، يكون التأثير على الأشخاص قاتلاً، حيث تشير التجارب المخبرية إلى أن تعرض حيوانات التجربة لمستوى ppm 5 لا يؤدي إلى أي ضرر . مما يشير إلى أن التأثير المباشر السام لغاز ثاني أوكسيد الكبريت يكون عند مستويات مرتفعة، إلا أن SO2 في الغلاف الجوي يعتبر من المركبات المؤدية إلى العديد من الحوادث الخطيرة. حيث يعزى لهذا الغاز، التسبب بالتسممات الحادة التي يسببها استنشاق الضباب الدخاني Smog في المدن الكبرى. ففي كانون الأول من عام 1930 حدث انقلاب حراري في بلجيكا أدى إلى راكم الفضلات الغازية للمصانع ووصل تركيز SO إلى ppm 38 مما أدى إلى وفاة 60 شخصاً بالاختناق ومقتل العديد من الماشية. وفي تشرين الأول من عام 1948 حدثت كارثة مشابهة في بنسلفانيا أدت إلى مرض 40% من سكان مدينة دونورا وموت 20 شخصاً، حيث كان تركيز ثاني أوكسيد الكبريت المقاس 2ppm. حادثة أخرى في لندن، عام 1952، حيث كان تركيز 2 SO فقط لايتجاوز 1.3ppm خلال خمسة أيام مع تصادفت حدوث إنقلاب حراري، أدى إلى ارتفاع عدد الوفيات ما بين 3500 . 4000 تقريباً زيادة عن معدلها الطبيعي، حيث أظهر التشريح وجود تخرشات بالجهاز التنفسي ومستويات مرتفعة من الكبريت في الجثث الميتة.
يزداد التأثير الضار لهذا الغاز عندما يتأكسد جزء منه ليتحول إلى غاز ثالث أوكسيد الكبريت SO الأشد سميةً من غاز ثاني أوكسيد الكبريت، بالإضافة إلى كونه يتحول لدى تماسه الماء إلى حمض الكبريت الأشد تشرداً من حمض الكبريتي.
إن عملية تحول ثاني أوكسيد الكبريت إلى ثالث أوكسيد الكبريت في الجو، هي عملية معقدة وتتم وفقا لآليتين مختلفتين:
1- تحدث الآلية الأولى نتيجة تفاعل كيميائي ضوئي Photochemical Process يتم في الطور الغازي ويكتسب بفضله غاز SO2 كمية معينة من الطاقة تأتي نتيجة تصادم الفوتونات في الاشعة فوق البنفسجية، وفقا للتفاعلين اللذين يؤديان إلى تشكل ثالث أوكسيد الكبريت والاوزون
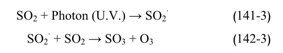
2- أما الآلية الثانية فتتلخص بالتفاعل الوساطي Catalytical Reaction الذي يتم ضمن قطيرات الطور السائل حيث تشكل بعض أملاح الحديد والمعادن الأخرى كالمغنيز Mn والموجودة في الغبار نواة تكاثف تعمل دور الوسيط في اتمام التفاعل.
3- كما يمكن تشكل ثالث أوكسيد الكبريت في أجواء المدن، حيث تنشط حركة مرور السيارات وذلك نتيجة الأكسدة المباشرة بواسطة تفاعل تسلسلي لفوق الأكاسيد RO2 بدءاً من جذور عضوية، وفقاً للتفاعل التالي:
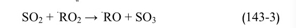
بالإضافة إلى تأثير ثاني أوكسيد الكبريت على الصحة، فإنه يؤثر بشكل مباشر على النباتات. حيث يؤدي إلى موت خلايا الأوراق عند تعرضها لتراكيز مرتفعة، و تدعى هذه الظاهرة بنخر الأوراق Leaf necrosis ، والتي يمكن تمييزها بالتلف الذي يحدث عند حواف الأوراق وعروقها بالإضافة إلى أن تعرض النباتات الحاد لغاز ثاني أوكسيد الكبريت يؤدي إلى زوال الاخضرار Chlorosis (قصر أو اصفرار للأوراق الخضراء). ويزداد خطر إصابة النباتات أثناء ضوء النهار وبازدياد الرطوبة، حيث تكون مسام الأوراق Stomata .متفتحة يؤدي تعرض المحاصيل الزراعية لمستويات منخفضة من غاز ثاني أوكسيد الكبريت لأزمنة طويلة، لانخفاض المردود خاصةً من القمح والشعير. يتحول غاز ثاني أوكسيد الكبريت في الغلاف الجوي إلى حمض الكبريت بذلك فإنه في المناطق المعرضة للتلوث بكميات كبيرة من SO2، تتخرب النباتات نتيجة التعرض لقطيرات حمض الكبريت، وذلك بظهور بقع على الأوراق في المناطق التي تسقط عليها هذه القطيرات. حيث يمكن أن تظهر أعراض التأثر بغاز SO2 على بعض الأنواع بمجرد أن يصل تركيزه الجوي إلى حدود ضئيلة جداً (جزءاً من المليون). بعض هذه النباتات الحساسة لغاز ثاني أوكسيد الكبريت هي: نباتات الفصيلة المظلية، والفصيلة الكستنائية، والفصيلة البقولية والكرمة، ونباتات الفصيلة الوعائية، بالإضافة إلى بعض الأشجار المثمرة. حيث استنبط حديثاً طريقة في علم البيئة لاختبار مدى تلوث الهواء بثاني أوكسيد الكبريت، تعتمد على مدى حساسية بعض النباتات لهذا الغاز. إذ تبين أن وجود غاز ثاني أوكسيد الكبريت يصبح مبيداً لكل من الطحالب والحزاز عندما يصبح تركيزه أعلى من 0.018 جزءاً من المليون. في حين أن التركيز المميت للنباتات الوعائية يتراوح بين 0.17 و 1 جزءاً من المليون. من ناحية أخرى، أهم تأثيرات التلوث بغاز ثاني أوكسيد الكبريت، هي تدهور وتآكل الأبنية وبعض أنواع المعادن، خاصةً معدن الزنك الذي يستخدم في تغطية سطوح المنازل، من الممكن أن يتفاعل كل من الرخام، أو الحجر الكلسي، حيث تتكون فلزاتها من كربونات الكالسيوم أو الدولوميت Dolomite المكون من كربونات الكالسيوم والمغنيزبوم، والتي تتفاعل مع غاز ثاني أوكسيد الكبريت الجوي لتنتج إما مواد منحلة أو قشور ضعيفة الالتصاق على المادة الصخرية، حيث تظهر تأثيرها العكسي على بنية، وسلامة، وعمر، ومظهر البناء. وبالرغم من أن كل من SO2 و NO تتفاعل مع الصخور، إلا أن التحاليل الكيميائية لقشور هذه الصخور، تبين أن غالبية الأملاح هي من أملاح الكبريت يتفاعل الدولوميت مع غاز ثاني أوكسيد الكبريت الجوي وفقاً للتفاعل:
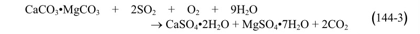
أخيراً، لا بد من الإشارة إلى أن ارتفاع تركيز ثاني أوكسيد الكبريت في الهواء، يؤدي إلى زيادة حموضة ماء المطر ، وبالتالي حموضة المياه الجارية والبحيرات والتربة. تدعى هذه الظاهرة بالأمطار الحامضية، والتي ينتج عنها نقص في إنتاج الثروة السمكية،


|
|
|
|
دخلت غرفة فنسيت ماذا تريد من داخلها.. خبير يفسر الحالة
|
|
|
|
|
|
|
ثورة طبية.. ابتكار أصغر جهاز لتنظيم ضربات القلب في العالم
|
|
|
|
|
|
|
العتبة العباسية المقدسة تستعد لإطلاق الحفل المركزي لتخرج طلبة الجامعات العراقية
|
|
|